在共价BTK抑制剂治疗失败的CLL/SLL患者中,LOXO-305治疗总缓解率高达84%。

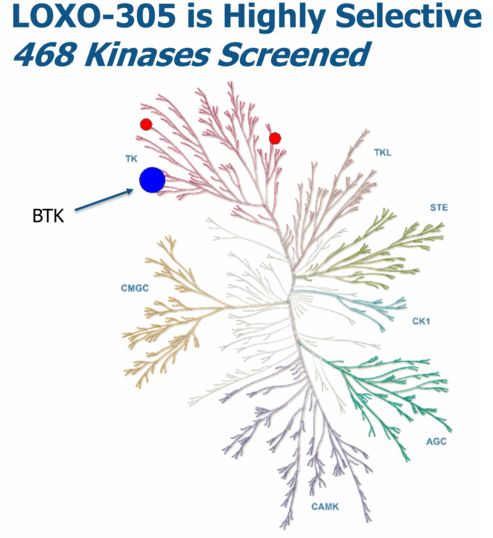
2020年12月08日讯 /生物谷BIOON/ --礼来(Eli Lilly)旗下肿瘤学公司Loxo Oncology近日在第62届美国血液学会(ASH)年会上公布了靶向抗癌药LOXO-305治疗慢性淋巴细胞白血病(CLL)和小细胞淋巴瘤(SLL)全球性1/2期BRUIN临床试验的最新数据。LOXO-305是一种研究性、高度选择性、非公价、布鲁顿酪氨酸激酶(BTK)抑制剂。
数据显示,在既往接受过BTK抑制剂治疗的CLL/SLL患者中,总缓解率(ORR)为62%,在随访10个月或更长时间的患者中,ORR提高至84%,无论先前BTK抑制剂停药原因或BTK突变状态如何,ORR具有一致性。在先前接受过所有类别可用疗法(化疗、抗CD20抗体、BTK抑制剂、BCL2抑制剂、PI3Kδ抑制剂)的患者中,观察到相似的ORR。在病情获得缓解的患者中,有94%仍维持缓解且仍在治疗。
会议报告者、纪念斯隆-凯特琳癌症中心CLL项目主任Anthony Mato医学博士表示:“在ASH上发表的数据揭示了LOXO-305在过度预治疗(heavily pre-treated,指先前接受过多种疗法)的CLL和SLL患者中具有令人鼓舞和一致的安全性和有效性,无论之前的疗法、这些疗法的中断原因或是否存在耐药性突变。对于先前接受过共价BTK抑制剂治疗的患者,我们越来越需要新的疗法,LOXO-305可能允许我们在尝试更复杂的治疗方法之前继续在同一生物类别的药物中治疗患者。”
Loxo Oncology首席医学官David Hyman表示:“LOXO-305的数据继续超出我们的预期,我们对这些数据对CLL和SLL患者意味着什么感到非常兴奋。这些新的数据进一步证实了我们的论点,即该药物的可逆结合模式、高选择性和强大的药理学为B细胞白血病和淋巴瘤提供了一个有差异化的治疗选择。我们期待在2021年启动3期项目。”
ASH年会上公布的关键数据包括:截止2020年9月27日,研究共入组323例患者,包括170例CLL/SLL患者、61例套细胞淋巴瘤(MCL)患者、26例华氏巨球蛋白血症(WM)患者、66例其他B细胞淋巴瘤患者。CLL/SLL患者既往接受的治疗方案中位数为3种,86%接受过BTK抑制剂治疗、90%接受过抗CD20抗体治疗、82%接受过化疗、34%接受过venetoclax(BCL-2抑制剂)治疗、21%接受过PI3K抑制剂、6%接受国CAR-T治疗、2%接受过异基因移植。
剂量递增阶段的药代动力学分析表明,在每天25mg到300mg的整个剂量范围内,剂量-比例暴露显示出一致性,患者间变异性较低。在整个给药间隔内,每天一次100mg及以上的剂量超过BTK IC90目标覆盖率。从首个剂量水平开始就观察到了治疗反应。
ASH的疗效数据基于研究的缓解评估。在所有剂量水平治疗的139例CLL/SLL患者中,88例病情缓解,包括69例部分缓解(PR)、19例淋巴细胞增多的部分缓解(PR-L)、45例疾病稳定(SD)、1例进行性疾病(PD),5例在首次疗效评估前停药,被认为不可评估(NE)。结果显示:总缓解率(ORR)为63%(95%CI:55-71)。
ORR在不同CLL/SLL患者亚组中是一致的,包括:(1)在121例可评估疗效的BTK预治疗患者中,ORR为62%(95%CI:53-71),随访10个月或更长时间的患者,ORR上升到84%(21/25)。随着时间的推移,这种反应的加深与其他BTK抑制剂是一致的,这表明LOXO-305的总体疗效将随着进一步的随访而继续增强。(2)先前因疾病进展而停用共价BTK抑制剂的患者ORR(67%[53/79])与因毒性或其他原因停止治疗的患者(52%[22/42])具有相似性。(3)携带BTK C481突变的患者ORR(71%[17/24])与无BTK C481突变的患者ORR(66%[43/65])也相似。(4)在先前接受过化学免疫、共价BTK抑制剂、BCL-2抑制剂治疗的患者中ORR为69%(27/39)。(5)在先前接受过所有5类CLL/SLL可用疗法(包括化学免疫治疗、共价BTK抑制剂、BCL-2抑制剂、PI3K抑制剂)治疗的患者中ORR为58%(7/12)。(6)在28例17p缺失、TP53突变或两者兼而有之的患者中ORR为79%(22/28)。
截至数据截止日期,88%的CLL/SLL患者仍在接受LOXO-305治疗。疗效可评估CLL/SLL患者的中位随访时间为6个月。在88例病情缓解的CLL/SLL患者中,除了5例患者(4例进展,1例PR并选择停止进行移植),其余均在继续接受治疗。随访时间最长的缓解患者在17.8个月时继续治疗。
会上报告提供了整个入组BRUIN研究人群的安全性数据。在这项研究中入组的323例患者中,最常见的不良事件是疲劳(20%)、腹泻(17%)和挫伤(13%)。此外,通常与BTK抑制剂相关的2种不良事件,即房性心律失常和出血的发生率较低,分别发生在2例患者和1例患者身上,研究人员认为与LOXO-305无关。在8%、2.2%和1.5%的患者中观察到药物相关不良事件的剂量中断、减少和永久停药。没有剂量限制性毒性报告,也没有达到最大耐受剂量(MTD)。
LOXO-305由美国肿瘤学精准药物开发公司Loxo Oncology发现,礼来在今年1月初以80亿美元将其收购。LOXO-305是一种研究性、高度选择性、非共价的布鲁顿酪氨酸激酶(BTK)抑制剂。BTK在B细胞抗原受体信号传导途径中起着关键作用,是正常白细胞(B细胞)和恶性B细胞发育、活化和生存所必需的。BTK是一个有效的分子靶点,在许多B细胞白血病和淋巴瘤中发现,包括慢性淋巴细胞白血病(CLL)、Waldenstrom巨球蛋白血症、套细胞淋巴瘤(MCL)和边缘区淋巴瘤(MZL)。
目前可用的BTK抑制剂不可逆地抑制BTK,这些疗法的长期疗效受到获得性耐药的限制,最常见的是通过BTK C481突变,以及由于对其他细胞靶点的非靶向抑制而产生的不耐受。LOXO-305被设计成可逆结合BTK,在C481获得性耐药突变的情况下保持活性,同时避开其他共价和非共价BTK抑制剂开发牵涉的非靶向激酶。
除了先前宣布的3期MCL试验外,Loxo Oncology正在准备对BTK预治疗的CLL/SLL患者启动2项全球随机3期临床试验(BRUIN CLL-321,BRUIN CLL-322),探索LOXO-305作为单药疗法及与其他药物的组合疗法。此外,Loxo Oncology还计划在2021年晚些时候启动一项全球随机头对头优越性3期研究,将LOXO-305与全球获批的首个BTK抑制剂Imbruvica(中文商品名:亿珂,通用名:ibrutinib,伊布替尼)一线治疗CLL/SLL进行对比。(生物谷Bioon.com)
原文出处:Loxo Oncology at Lilly Announces Updated Data from the Phase 1/2 BRUIN Clinical Trial for LOXO-305 in Chronic Lymphocytic Leukemia and Small Lymphocytic Lymphoma at the American Society of Hematology Annual Meeting